112年:(醫檢)生化(2)
下列何者是應用實驗室開發檢測技術( LDTs )和體外診斷器材( IVD )檢驗的主要差異?
A衛生主管機關查驗登記
B方法查證與確效流程
C品質控制( quality control )方式
D結果臨床判讀( clinical interpretation )
詳細解析
本題觀念:
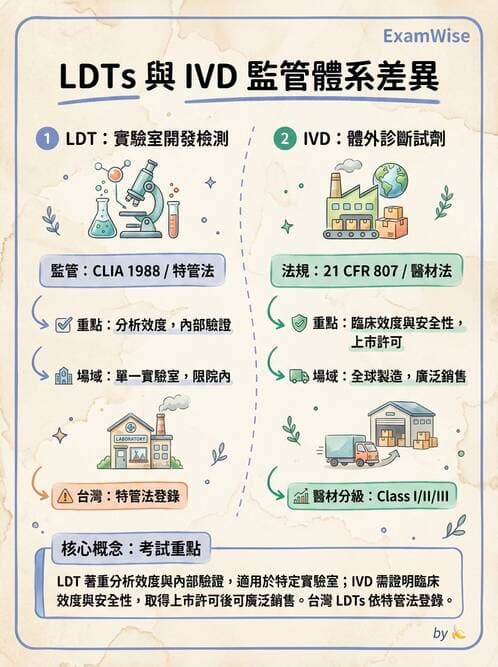
探索實驗室自行開發檢測(LDTs)與商業化體外診斷器材(IVD)在法規監管與查驗登記上的差異。LDTs 由臨床實驗室依 CLIA 規範內部設計、製造、驗證並執行;IVD 則由製造商依 FDA(或我國 TFDA)相關規定完成註冊、預市場審查與品質系統法規(QSR)等一系列查驗登記程序。
選項分析
- 選項A 衛生主管機關查驗登記
IVD 必須於上市前完成衛生主管機關(如美國 FDA 或我國 TFDA)之醫療器材查驗登記與上市許可(21 CFR 807.20)。LDTs 雖屬體外診斷產品,但因在單一 CLIA 認證實驗室內自行研發、製造與使用,傳統上不需向 FDA 申請裝置註冊或上市許可,僅須符合 CLIA 的方法驗證與品質控制規範 (fda.gov),我國 MOHW 亦另行設立「實驗室開發檢測登錄管理系統」,與醫療器材查驗登記制度分屬不同管理模式 ([dep.mohw.gov.tw](https://dep.mohw.gov.tw/DOMA/cp-5177-77072-106.html?utm_source
...(解析預覽)...
升級 VIP 解鎖圖文解析