110年:(醫檢)生化(2)
根據 Michaelis-Menten kinetics ,在一酵素反應中,若出現競爭性抑制劑,對此反應的影響為:
AKm不變,Vmax變大
BKm不變,Vmax變小
CVmax不變,Km變大
DVmax不變,Km變小
詳細解析
本題觀念:
本題考查的是酵素動力學(Enzyme Kinetics)中,競爭性抑制(Competitive Inhibition) 對 Michaelis-Menten 參數( 和 )的影響。這是醫學檢驗師在生物化學與臨床酵素學中必須掌握的基礎觀念。
選項分析
- A. Km不變,Vmax變大:錯誤。
- 競爭性抑制劑不會增加反應的最大速率。
- B. Km不變,Vmax變小:錯誤。
- 這通常是**非競爭性抑制(Non-competitive inhibition)**的特徵(指抑制劑可與游離酵素 E 或酵素-基質複合物 ES 結合,且親和力相等的情況)。
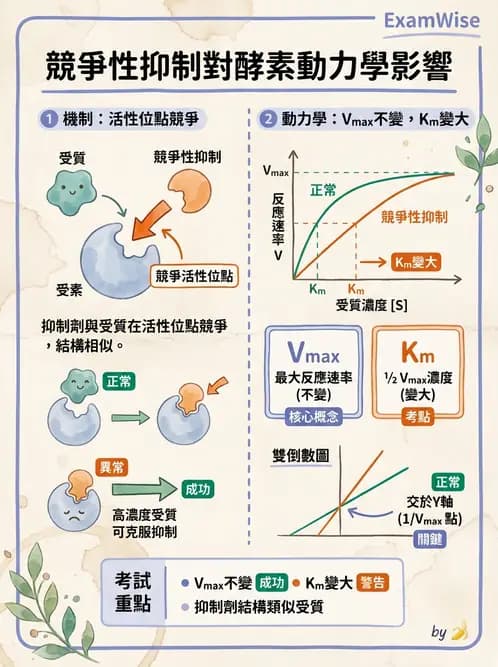
- C. Vmax不變,Km變大:正確。
- 機制:競爭性抑制劑(Inhibitor, I)的結構與受質(Substrate, S)相似,會與受質競爭酵素(Enzyme, E)的活性位點(Active site)。
- 對 的影響:由於抑制劑與酵素的結合是可逆的,只要加入足夠高濃度的受質,受質就能「競爭」過抑制劑,佔據所有的活性位點。因此,反應最終仍能達到原本的最大速率(),即 不變。
...(解析預覽)...
升級 VIP 解鎖圖文解析