111年:醫物幅安(2)
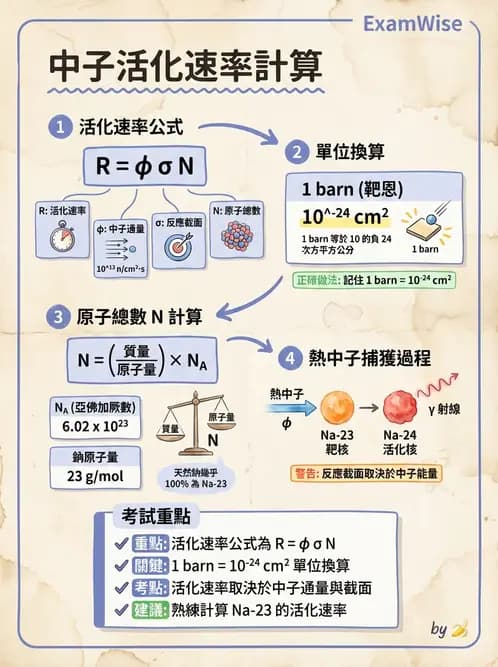
原子爐內發生23Na (n,γ)24 Na反應,其熱中子捕獲截面 σ=0.53 b ,若入射熱中子通量密度為 1013neutrons/cm2*sec,則每克 Na的活化速率( activations/g*sec )為多少?
A1.38×107
B1.38×1011
C3.19×108
D3.19×1012
詳細解析
本題觀念:
本題測驗中子活化(Neutron Activation)的基本計算。當靶物質放置於反應爐的中子通量場中,靶原子核會捕獲中子而發生核反應(如本題的熱中子捕獲反應 ),進而轉變為放射性同位素。單位時間內生成的放射性核種數量即為「活化速率(Activation rate)」。
計算活化速率 的核心公式為: 其中:
- :入射中子通量密度(Neutron flux density),單位為 。
- :反應截面(Cross-section),代表核反應發生的機率。1 靶恩(barn, b) 。
- :靶物質的原子數量(Number of target atoms)。
選項分析
- A:計算結果數量級錯誤,可能源於未將靶恩(barn)正確換算為 ,或是未能正確運用亞佛加厥常數。
- B:正確。透過公式 計算得出 ,詳細計算步驟請見答案解析。
- **C
...(解析預覽)...
升級 VIP 解鎖圖文解析