109年:(醫檢)生化(1)
一病人動脈血之重碳酸鹽濃度為 25 mmol/L ,二氧化碳分壓低於正常值,且重碳酸鹽與溶解的二氧化碳濃度之比值為 25 :1,則此病人是下列何種狀況?( pH=7.4 時,重碳酸鹽與溶解的二氧化碳濃度之比值為 20 :1)
A呼吸性酸中毒
B呼吸性 鹼中毒
C代謝性酸中毒
D代謝性 鹼中毒
詳細解析
本題觀念:
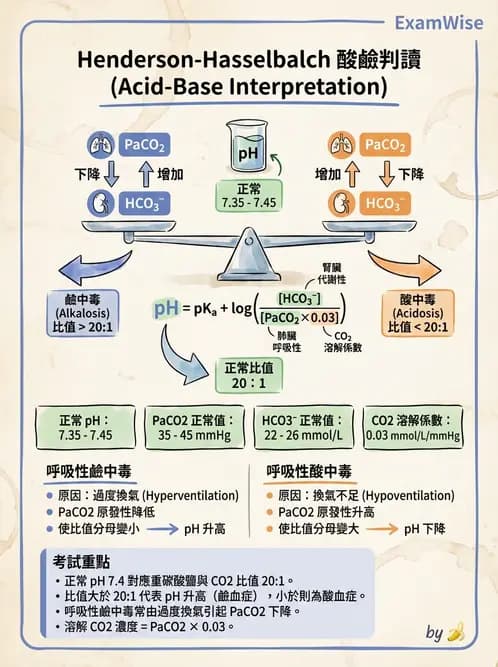
本題考核 Henderson-Hasselbalch 方程式在酸鹼判讀中的應用。pH 由 與溶解 ()的比值決定,正常比值為 20:1(對應 pH 7.4)。比值升高表示鹼性偏移,而此題需判斷是哪一種酸鹼異常。
選項分析
題目給定條件:
- = 25 mmol/L(正常範圍 22–26 mmol/L)
- 低於正常值(正常 35–45 mmHg)
- : 溶解 比值 = 25:1(正常 pH 7.4 時為 20:1)
利用 Henderson-Hasselbalch 方程式:
當比值 = 25:1 > 正常 20:1:
...(解析預覽)...
升級 VIP 解鎖圖文解析