108年:(醫檢)生化(2)
病患血液氣體分析結果 pH 7.1 、PCO₂ 80 mmHg ,則血中重碳酸鹽( Bicarbonate )濃度約為多少 mEq/L ? 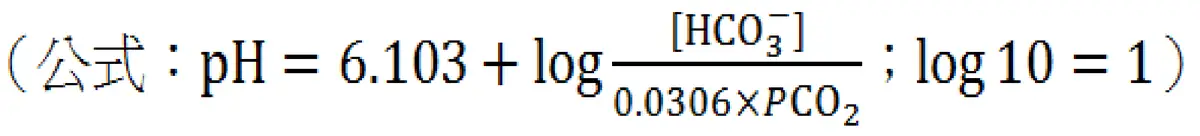
A10
B16
C24
D36
詳細解析
本題觀念:
本題考查 Henderson-Hasselbalch 方程式的應用,利用已知的 pH 和 反推血中重碳酸鹽(bicarbonate, )濃度。題目圖片提供的公式為:
此為 Henderson-Hasselbalch 方程式在血液氣體分析中的具體應用形式,其中:
- 6.103 為碳酸的 pKa(亦常以 6.1 近似使用)
- 0.0306(或常見近似值 0.03)mmol/L/mmHg 為 在血漿中的溶解度係數
- 單位為 mEq/L
- 單位為 mmHg
影像分析:
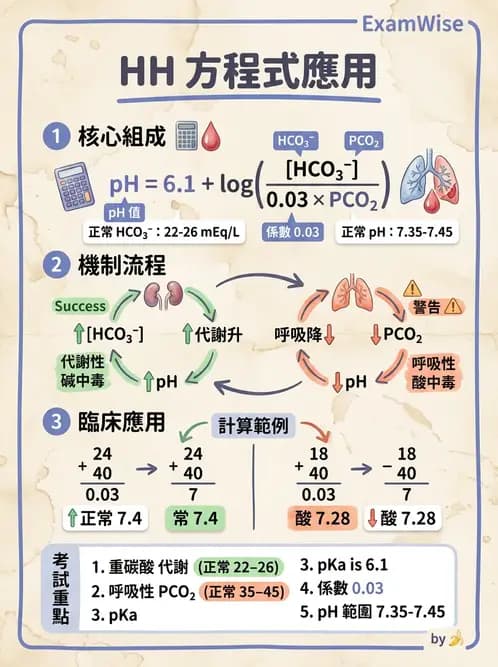
題目所附圖片顯示解題所需之公式:
此公式即 Henderson-Hasselba
...(解析預覽)...
升級 VIP 解鎖圖文解析