107年:(醫檢)生化(2)
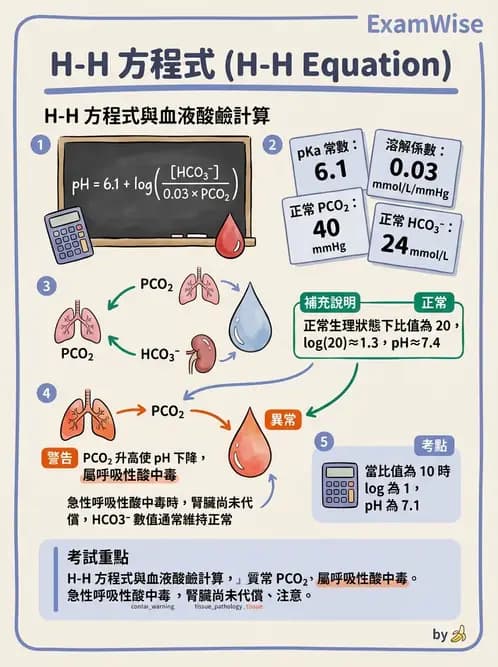
血液氣體分析 PCO 2為80 mmHg ,HCO₃⁻為24 mmol/L 時,血液之 pH 約為下列何者?(公式: pH =pKa +log【bicarbonate /pCO2 × 0.03 】)
A6.1
B6.8
C7.1
D7.8
詳細解析
本題觀念:
利用 Henderson-Hasselbalch 方程式計算血液 pH,以及呼吸性酸中毒(respiratory acidosis)的判讀。
選項分析
(A) 6.1 6.1 是 Henderson-Hasselbalch 方程式中的 pKa 值,而非計算所得的 pH,此選項錯誤。
(B) 6.8 計算結果與此值不符,此選項錯誤。
(C) 7.1 正確。代入計算後得 pH = 7.1(詳見答案解析)。
(D) 7.8 pH > 7.45 為鹼中毒(alkalosis),但本題 大幅升高(80 mmHg),符合呼吸性酸中毒,pH 必定偏低,此選項明顯錯誤。
答案解析
答案為 (C) 7.1。
題目給定公式為:
代入數值:
- pKa = 6.1
- = 24 mmol/L
- = 80 mmHg
計算步驟:
...(解析預覽)...
升級 VIP 解鎖圖文解析