107年:核醫診療(2)
硫-36 (Z=16 )與氯-37 (Z=17 )互為:
A同位素(isotope )
B同中子數( isotone )
C同重數(isobar )
D核異構物( nuclear isomer )
詳細解析
本題觀念:
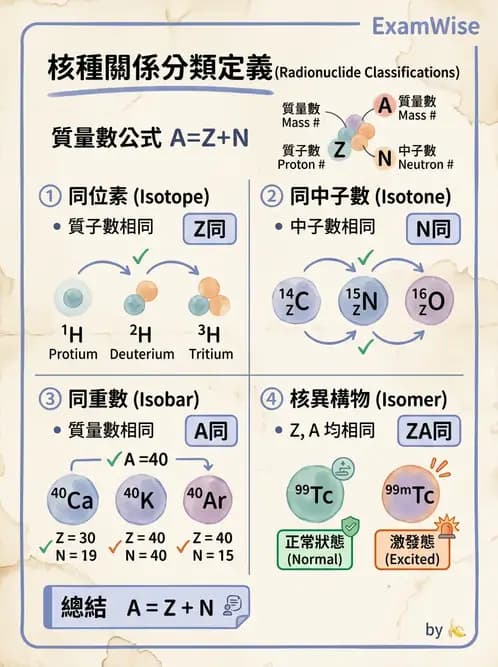
本題考核核物理中描述原子核組成關係的基本術語:同位素(isotope)、同中子數(isotone)、同重數(isobar)、核異構物(nuclear isomer)。判斷關鍵在於比較兩核種的質子數(Z)、中子數(N)和質量數(A)。
各術語定義整理:
| 術語 | 相同 | 不同 |
|---|---|---|
| 同位素(isotope) | Z(質子數) | A、N |
| 同中子數(isotone) | N(中子數) | Z、A |
| 同重數(isobar) | A(質量數) | Z、N |
| 核異構物(nuclear isomer) | Z 和 A 均相同 | 核能態(激發 vs. 基態) |
選項分析
首先計算兩核種的中子數:
- 硫-36(S): 個中子
- 氯-37(Cl): 個中子
兩者的質子數不同(16 ≠ 17),質量數不同(36 ≠ 37),但中子數相同(均為 20)。
(A) 同位素(isotope) 同位素需具備相同的質子數(Z)。S 的 Z=16,Cl 的 Z=17,兩者 Z 不同。*
...(解析預覽)...
升級 VIP 解鎖圖文解析