106年:醫物幅安(2)
已知鉛的密度為 11.3 g/cm³,原子量為 207.21 g ,試問每cm³之鉛所含原子數為多少?
A2.9×10²²
B3.3×10²²
C3.3×10²³
D3.5×10²³
詳細解析
本題觀念:
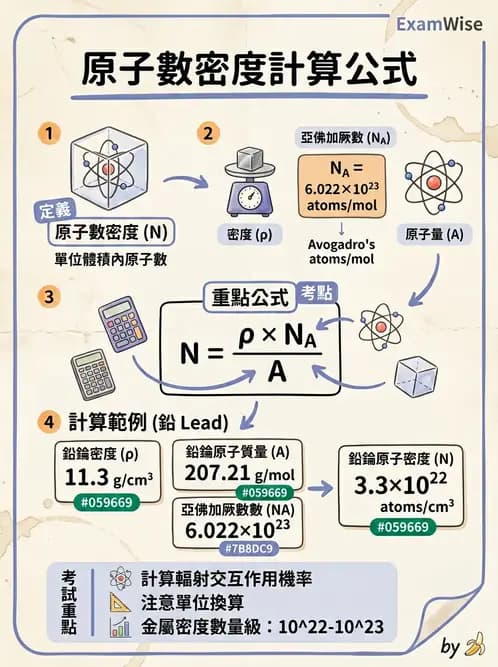
本題考查原子數密度(atomic number density)的計算,這是核物理與輻射防護的基礎計算。利用物質密度、原子量(莫耳質量)和亞佛加厥數(Avogadro's number)求每單位體積中的原子數。
選項分析
計算公式:
其中:
- :每 的原子數(atoms/cm³)
- :密度(g/cm³)= 11.3 g/cm³
- :亞佛加厥數(Avogadro's number)= atoms/mol
- :原子量(g/mol)= 207.21 g/mol
代入計算:
(A) → 錯誤,數值偏小。
(B) → 正確,與計算結果 $3.28 \times 10
...(解析預覽)...
升級 VIP 解鎖圖文解析