109年:護理基礎醫學(2)
一莫耳葡萄糖(即180克)溶解於1公升水中所產生的滲透壓濃度為多少Osmol/L?
A1
B2
C3
D4
詳細解析
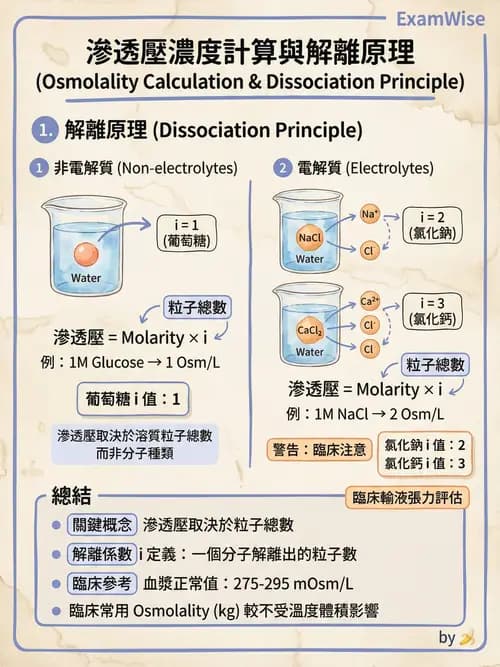
本題觀念:Osmolarity(滲透壓濃度)的計算
Osmolarity 指的是每一公升溶液中「可產生滲透壓作用的粒子數目」,單位為 Osmol/L。
公式:Osmolarity (Osmol/L) = molar concentration (mol/L) × 顆粒數 (i)
• 非電解質(不解離):i = 1
• 電解質(會電離):i ≧ 2,視解離後粒子數而定,如 NaCl ≈ 2、CaCl₂ ≈ 3。
本題關鍵:Glucose 為非電解質,溶於水後不解離。
選項分析
A. 1 Osmol/L ← 正確。1 mol/L × i(=1) = 1 Osmol/L。
B. 2 Osmol/L → 需要二價解離(如 1 mol/L NaCl 理想值)。
C. 3 Osmol/L → 需三粒子(如 1 mol/L CaCl₂)。
D. 4 Osmol/L → 四粒子或更高解離才可能(臨床少見)。
答案解析
題目給出:1 mol glucose (180 g) 溶於 1 L 水,即濃度 1 mol/L。
Glucose 不解離,i = 1,故:
Osmolarity = 1 mol/L × 1 = 1 Osmol/L。
因此選 A。
知識整合與臨床重要性
- 生理液體滲透壓約 275–295 mOsm/kg(mOs
...(解析預覽)...
升級 VIP 解鎖圖文解析