113年:(醫檢)生化(1)
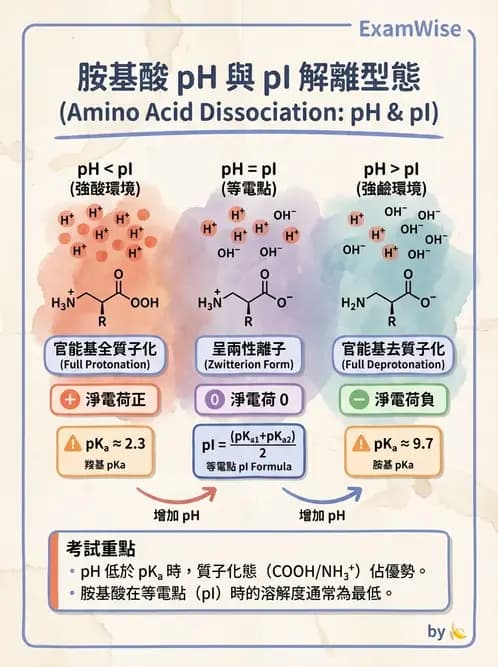
當pH遠低於pI時,胺基酸的官能基主要呈現下列何種解離型態?
A-NH₂ 及 -COO⁻
B-NH₂ 及 -COOH
C-NH₃⁺ 及 -COOH
D-NH₃⁺ 及 -COO⁻
詳細解析
本題觀念:
本題探討胺基酸(amino acid)在不同pH值下的解離型態,核心在於等電點(isoelectric point, pI)的意義及pH與pI的比較如何影響胺基(–NH2/–NH3+)與羧基(–COOH/–COO–)的質子化狀態。
選項分析
-
選項A:–NH2 及 –COO–
在中性或等電點附近,胺基酸以兩性離子(zwitterion,–NH3+ 與 –COO–)最穩定;pH大於pI時,–NH3+ 失去質子變成 –NH2,–COO– 保持去質子形態。但本題假設pH遠低於pI,環境極酸性,不符合僅出現 –NH2 與 –COO– 的情況,因此排除。 -
選項B:–NH2 及 –COOH
在極高pH下(遠大於pI)時,–COOH 會失去質子變成 –COO–,而–NH3+ 也可能失去質子,但在低pH條件下,–NH2 不會保持未質子化,故此組合不合題意,排除。 -
選項C:–NH3+ 及 –COOH
當pH遠低於pI(酸性環境),溶液中H+濃度高,首先使羧基–COO–得質子成為–COOH,同時胺基–NH2易被質子化為–NH3+,兩官能基皆處於質子化態,胺基酸帶正電,此組合正確。([chem.libretexts.org](https://chem.libretexts.org/Courses/University_of_Ke
...(解析預覽)...
升級 VIP 解鎖圖文解析