115年:營養生理生化(1)
根據琥珀酸(succinate)的化學結構式(如圖所示),下列何者最可能為琥珀酸去氫酶(succinate dehydrogenase)作用於琥珀酸的競爭型抑制劑(competitive inhibitor)? 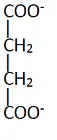
A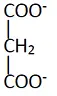
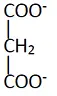
B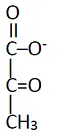
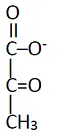
C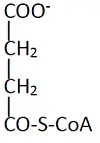
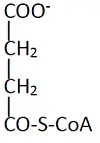
D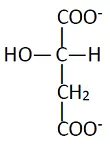

詳細解析
本題觀念:
本題考查生物化學中三羧酸循環 (TCA cycle) 的關鍵酵素——琥珀酸去氫酶 (Succinate Dehydrogenase, SDH) 及其競爭型抑制劑 (Competitive Inhibitor) 的結構與機制。
核心機制:
- 琥珀酸去氫酶 (SDH):負責催化琥珀酸 (Succinate) 氧化生成富馬酸 (Fumarate),同時將 FAD 還原為 FADH2。這是 TCA 循環中唯一結合在粒線體內膜上的酵素(亦即電子傳遞鏈的 Complex II)。
- 競爭型抑制:抑制劑與受質 (Substrate) 的化學結構非常相似,因此會競爭酵素的活化位 (Active site)。抑制劑結合後,因結構差異無法進行後續催化反應,從而阻斷酵素活性。
影像分析:
-
題目圖片 (Substrate):
- 結構:顯示一個二羧酸分子,中間有兩個亞甲基 (-CH2-CH2-)。
- 鑑定:這是 琥珀酸 (Succinate),化學式為 。
-
選項圖片解析:
- 選項 A:
- 結構:顯示一個二羧酸分子,中間只有一個亞甲基 (-CH2-)。
- 鑑定:這是 丙二酸 (Malonate)。
- 選項 B:
- 結構:三碳分子,含一個酮基 (C=O) 與一個羧基。
- 鑑定:這是 丙酮酸 (Pyruvate)。
- 選項 C:
- 結構:四碳骨架兩端羧基,其中一端透過硫酯鍵接 CoA。
- 鑑定:這是 琥珀醯輔酶 A (Succinyl-CoA)。
- 選項 D:
- 結構:四碳二羧酸,C2 位帶一個羥基 (OH)。
- 鑑定:這是 蘋果酸 (L-Malate)。
- 選項 A:
選項分析
-
選項 A (丙二酸 Malonate):正確答案。
- 結構相似性:丙二酸與琥珀酸都帶有兩個帶負電的羧基 (),且分子大小相近。琥珀酸主要骨架有兩個碳 (),而丙二酸只有一個碳 ()。
- 抑制機制:丙二酸能完美嵌入琥珀酸去氫酶的活化位(因為羧基間距相似),但由於缺乏兩個相鄰的亞甲基,無法發生去氫反應(無法形成雙鍵),因此「卡住」了酵素,是教科書中最經典的 SDH 競爭型抑制劑。
-
選項 B (丙酮酸 Pyruvate):
- 結構為三碳單羧酸,與琥珀酸的四碳雙羧酸結構差異大,不是 SDH 的競爭型抑制劑。屬於糖解作用末端產物,會進入 TCA 循環之前由 PDH 轉成 acetyl-CoA。
-
選項 C (琥珀醯輔酶 A Succinyl-CoA):
- 這是琥珀酸的前驅物(在 Succinyl-CoA synthetase 作用下生成琥珀酸 + GTP)。它是 SDH 受質的前一步代謝物,並非抑制劑。
-
選項 D (蘋果酸 L-Malate):
- 為 TCA 循環中 fumarate 之後的下一步代謝物,由 fumarase 催化加水形成。雖然也是四碳二羧酸,但碳骨架含羥基(–OH),與琥珀酸(–CH₂–CH₂–)結構不同,不是 SDH 的主要競爭型抑制劑。
答案解析
琥珀酸 (Succinate) 的結構特徵是兩個羧基中間隔著兩個亞甲基 ()。琥珀酸去氫酶的作用是在這兩個碳之間移除氫原子形成雙鍵。
丙二酸 (Malonate, 選項 A) 的結構是兩個羧基中間隔著一個亞甲基 ()。這種結構上的高度相似性(Structural Analog)使其能與酵素的活化位結合,但因碳鏈長度不足,無法進行脫氫反應。因此,丙二酸會與琥珀酸競爭酵素結合位,增加 值但不改變 ,符合競爭型抑制劑的動力學特徵。
因此,最可能的競爭型抑制劑為 A (丙二酸)。
核心知識點
- 經典考點:Succinate Dehydrogenase 的競爭型抑制劑 = Malonate (丙二酸)。
- 酵素動力學:競爭型抑制劑 (Competitive Inhibitor) 特徵為:
- 結構類似受質。
- 與受質競爭活化位 (Active site)。
- 不變(受質濃度夠高可克服抑制)。
- 上升(親和力看似下降)。
- Complex II:SDH 是電子傳遞鏈中唯一不具備質子泵 (Proton pump) 功能的複合體,直接將電子傳遞給 CoQ。
參考資料
- Lehninger Principles of Biochemistry, "Citric Acid Cycle", Enzyme Inhibition sections.
- Harper's Illustrated Biochemistry, "Biologic Oxidation".