112年:營養生理生化(2)
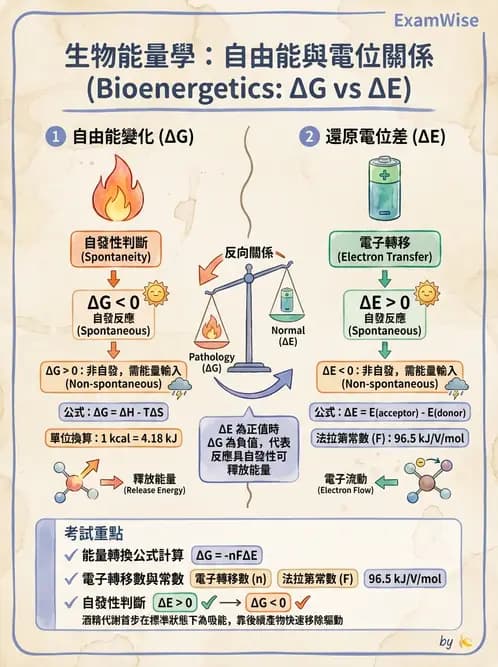
酒精在肝細胞中氧化代謝的反應式為:C₂H₅OH + NAD⁺→CH₃CHO + NADH + H⁺;此反應的還原電位變化ΔE'₀= -0.123 V 。已知反應自由能與電位之間的關係是ΔG'₀= -nFΔE'₀,其中n= 2,F= 96.5 kJ/V/mol 。已知1 kcal = 4.18 kJ 。計算此反應的ΔG'₀自由能變化值約為多少?
A-99 kcal/mol
B23.7 kJ/mol
C99.1 kcal/mol
D-5.67 kcal/mol
詳細解析
本題觀念:
生物能量學 (Bioenergetics)、氧化還原反應 (Redox Reaction)、吉布斯自由能 (Gibbs Free Energy)
本題考查的核心觀念是利用氧化還原電位 () 計算標準自由能變化 ()。這是生物化學中能量代謝的基礎計算,特別是在酒精代謝(乙醇 乙醛)的反應中,理解為何在標準狀態下非自發的反應,在細胞內卻能順利進行。
選項分析
計算步驟詳解:
-
確認公式: 題目給定公式 。
- :反應中轉移的電子數。酒精氧化為乙醛的過程涉及 2 個電子的轉移 (),故 。
- :法拉第常數 (Faraday constant),題目給定 。
- :標準還原電位變化,題目給定 。
-
代入數值:
\begin{aligned} \De
...(解析預覽)...
升級 VIP 解鎖圖文解析