110年:營養生理生化(1)
酸及鹼可以使蛋白質變性,主要是因為其可破壞蛋白質之:
A氫鍵及肽鍵
B鹽橋及氫鍵
C肽鍵及鹽橋
D鹽橋及疏水性交互作用
詳細解析
本題觀念:
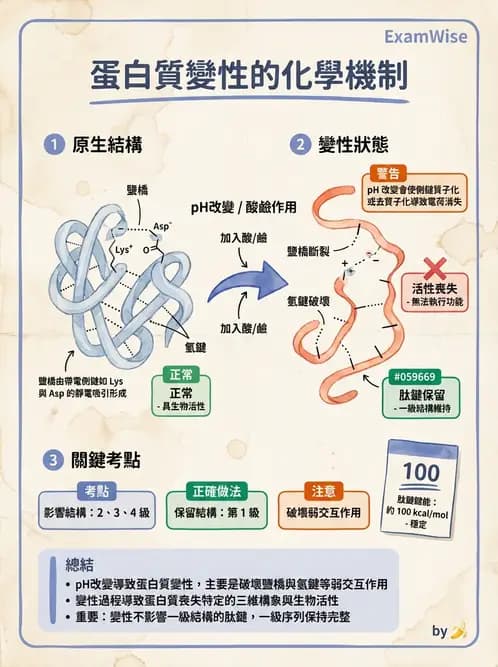
本題考查的是**蛋白質變性(Denaturation)**的化學機制,特別是針對「酸鹼(pH值改變)」對蛋白質結構中化學鍵結的影響。
- 變性的定義:蛋白質變性是指蛋白質受到物理或化學因素(如熱、酸鹼、有機溶劑、重金屬等)影響,導致其二級、三級或四級結構(立體構象)被破壞,失去生物活性,但一級結構(胺基酸序列/肽鍵)通常保持完整。
- 酸鹼的作用機制:酸鹼主要透過改變溶液中的氫離子濃度(pH值),影響胺基酸側鏈(R基團)的解離狀態(帶電性)。
選項分析
- A. 氫鍵及肽鍵:錯誤。
- 肽鍵(Peptide bond)是連接胺基酸形成一級結構的共價鍵,鍵能極強。一般的「變性」過程(如加熱、酸鹼處理)通常不會打斷肽鍵。打斷肽鍵需要「水解」(Hydrolysis),例如使用強酸高溫長時間煮沸或蛋白酶作用。因此選項中包含肽鍵者皆非主要變性機制。
- B. 鹽橋及氫鍵:正確。
- 鹽橋(Salt bridges):又稱離子鍵,是由帶正電(如 Lys, Arg, His)與帶負電(如 Asp, Glu)的胺基酸側鏈形成的靜電吸引力。酸鹼改變會直接改變這些基團的質子化狀態(例如加酸使 -COO⁻ 變為 -COOH,失去負電),導致電荷消
...(解析預覽)...
升級 VIP 解鎖圖文解析