106年:營養生理生化(2)
根據 Michaelis-Menten 酵素動力學的理論,下列敘述何者正確?
A穩定狀態假說認為酵素與受質的複合體濃度,在整個反應過程中幾乎維持恆定
B催化反應的一般速率常數 kcat可代表酵素與受質的鍵結能力
CMichaelis 常數 Km可說明在單位時間下,單位濃度的酵素水解多少受質
DKm / kcat解釋酵素的效率( efficiency )
詳細解析
本題觀念:
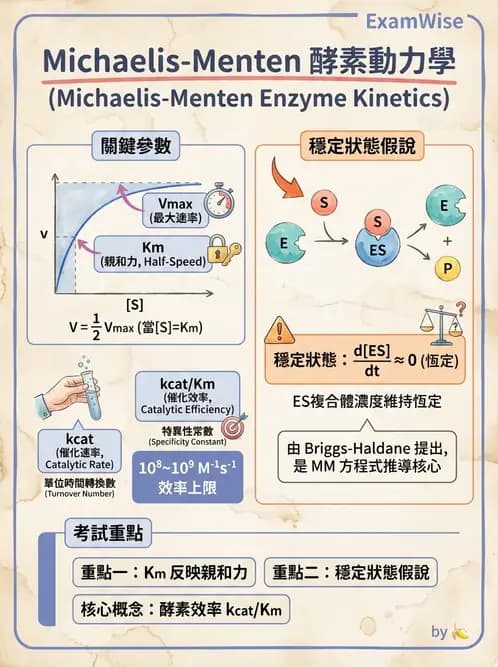
Michaelis-Menten 酵素動力學是描述酵素催化反應速率的基本理論,核心假說為「穩定狀態假說(steady-state assumption)」,由 Briggs 和 Haldane 提出——認為酵素-受質複合體(ES complex)的濃度在反應過程中幾乎維持恆定。Km、kcat 及 kcat/Km 各有其特定意義,不可混淆。
選項分析
(A) 穩定狀態假說認為酵素與受質的複合體濃度,在整個反應過程中幾乎維持恆定 正確。 穩定狀態假說(steady-state assumption)由 Briggs 和 Haldane(1925)提出,核心主張:ES complex 的生成速率等於其消耗速率,因此 在反應初始後幾乎維持不變()。此正是 Michaelis-Menten 方程式推導的基礎。此選項為正確答案。
(B) 催化反應的一般速率常數 kcat 可代表酵素與受質的鍵結能力 錯誤。 kcat(turnover number,催化轉換數)代表在受質飽和條件下,單位時間內每個酵素分子可將多少受質轉換為產物,反映的是催化速率,而非結合親和力。代表酵素與受質結合能力的參數是 Km(值愈小,親和力愈高)。
(C)
...(解析預覽)...
升級 VIP 解鎖圖文解析